
仿生纳米颗粒通过抑制HIF-1α/ P3通路缓解类风湿性关节炎
原名: Biomimetic Nanoparticles Inhibit the HIF-1α/iNOS/NLRP3 Pathway to Alleviate Rheumatoid Arthritis
译名: 仿生纳米颗粒通过抑制HIF-1α/iNOS/NLRP3通路缓解类风湿性关节炎
期刊: Nano Letter
影响因子: 9.6
发表时间: 2025.03.03
DOI:10.1021/acs.nanolett.4c05782
1 研究背景
类风湿性关节炎(RA)是一种慢性自身免疫性疾病,全球患病率为0.5%~1%。其主要特征是外周关节滑膜的炎症细胞浸润,导致滑膜增生、软骨丢失,甚至引发不可逆的残疾。RA的病理过程涉及多种细胞和分子机制:①滑膜炎症:滑膜细胞(尤其是成纤维样滑膜细胞,FLS)在炎症过程中过度增殖,分泌基质降解酶,破坏软骨和骨骼。②细胞间相互作用:滑膜细胞与浸润的炎症细胞(如巨噬细胞、T细胞)相互作用,释放促炎细胞因子(如TNF-α、IL-1β、IL-6)和基质降解因子,加剧炎症反应。③缺氧微环境:滑膜增生和炎症细胞浸润导致局部代谢增加,进一步加剧缺氧,放大炎症反应。
目前,RA的治疗主要依赖于非甾体抗炎药(NSAIDs)和生物制剂,但这些方法存在显著的局限性:①NSAIDs:通过抑制免疫系统的信号传导来减轻炎症,但长期使用可能导致严重的副作用,如胃肠道出血、肝损伤、心血管疾病等。②生物制剂:虽然在控制炎症方面表现出色,但价格昂贵,且可能引发感染等风险。③药物递送的挑战:许多具有抗炎潜力的药物(如天然黄酮类化合物槲皮素)由于其水溶性差、物理化学稳定性低以及细胞摄取能力弱,难以在病变部位实现有效富集,限制了其临床应用。
为克服传统药物递送系统的局限性,研究者们探索了细胞膜仿生纳米载体(biomimetic nanoparticles)的应用。细胞膜仿生纳米载体通过整合细胞膜蛋白,赋予纳米颗粒以下优势:①免疫逃逸:细胞膜蛋白的包裹使纳米颗粒能够逃避免疫系统的识别,延长其在体内的循环时间。②靶向递送:利用细胞膜蛋白的同源靶向性,纳米颗粒能够特异性地递送药物至病变部位,提高药物浓度,减少全身副作用。③多功能性:结合不同细胞膜蛋白,纳米载体还可以实现多种功能,如增强血管通透性、改善成像效果等。近年来,生物模拟纳米载体在多种疾病治疗中展现出巨大潜力,例如:抗肿瘤治疗、抗菌治疗、炎症性疾病治疗等。
槲皮素(chrysin)是一种天然黄酮类化合物,具有抗炎、抗氧化和免疫调节等多种药理活性。研究表明,槲皮素可以通过抑制NLRP3炎症体来缓解骨关节炎(OA)的疼痛。然而,槲皮素的临床应用受水溶性差、物理化学稳定性低、非选择性分布等限制。因此,开发一种能够高效递送槲皮素至炎症关节的纳米载体,对于提高其治疗效果具有重要意义。
基于此,该团队开发了一种基于FLS膜蛋白的细胞膜仿生纳米载体(FMPlipo@C),通过整合成纤维样滑膜细胞(FLS)膜蛋白与载药脂质体,实现槲皮素在RA炎症关节的靶向递送,抑制关键炎症通路(HIF-1α/iNOS/NLRP3),从而为RA的治疗提供一种高效、安全的新策略。
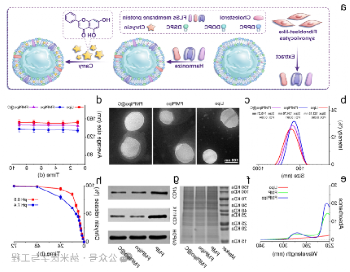
图1 FMPlipo@C的制备和表征
2 研究亮点及创新点
1.创新的生物模拟纳米载体设计:研究者利用成纤维样滑膜细胞(FLS)膜蛋白的同源靶向性,将FLS膜蛋白整合到纳米载体表面。这种设计使得纳米载体能够特异性地识别并结合到炎症关节中的FLS细胞,显著提高了药物在病变部位的富集效率,减少了全身副作用。这种基于细胞膜蛋白的靶向策略在RA治疗中具有创新性。通过整合FLS膜蛋白,纳米载体不仅实现了靶向递送,还具备了免疫逃逸的能力,延长了药物在体内的循环时间。同时,纳米载体的设计还考虑了药物的稳定性和释放特性,使其能够在酸性环境中(如炎症部位)快速释放药物。
2.跨学科研究方法:该研究将纳米材料的制备技术与生物学研究方法相结合,通过设计和优化纳米载体,实现了药物的高效递送和靶向治疗。这种跨学科的研究方法不仅推动了纳米技术在医学领域的应用,也为其他疾病的治疗提供了新的思路。